- Accueil
- volume 10 (2006)
- numéro 2
- Caractéristiques de la dormance des bourgeons du pommier dans les régions à hiver doux
Visualisation(s): 8658 (43 ULiège)
Téléchargement(s): 245 (2 ULiège)
Caractéristiques de la dormance des bourgeons du pommier dans les régions à hiver doux

Notes de la rédaction
Reçu le 1er avril 2004, accepté le 27 octobre 2005
Résumé
En vue de mieux comprendre la dormance des bourgeons en climat à hiver doux, l’évolution des capacités de débourrement a été établie, sur base du test « boutures de nœuds isolés », durant trois années successives. Les bourgeons ont été prélevés sur des pommiers Golden delicious croissant dans la région de Meknès (Maroc) où des problèmes de débourrement anormal surviennent de temps à autre. Les courbes de temps moyen de débourrement ainsi obtenues montrent une première phase d’inertie, faible et temporaire, d’origine corrélative, mais d’intensité variable d’une année à l’autre. Il y succède un pic de dormance vraie qui apparaît successivement induite, puis effacée par les températures basses de novembre à mars. Les désordres de débourrement proviennent de la conjonction d’une inertie initiale élevée, liée aux conditions de croissance antérieures, et de la brève période de froid de la région considérée. C’est donc, en fait, moins le manque de froid que la double action de froid, dont une part accentue la dormance avant de commencer à l’éliminer, qui est à mettre en cause.
Abstract
Evolution and characteristics of apple bud dormancy in mild winter conditions. In order to study bud dormancy in mild winter climate, the evolution of bud bursting capabilities was investigated, using the « one-node-cutting test », during three successive years. The buds were sampled from Golden delicious apple trees grown in the region of Meknes (Morocco), where now and then abnormal bud burst occurs. The made-up graphs of mean bursting time display a first phase of bud inertia, weak and temporary, of correlative origin, but variable from year to year. This is followed by a peak of true dormancy, wich appears first induced and afterwards removed by the chilling temperatures from november to march. The bud break disorders result thus from the combined effect of a high initial inertia, linked to the previous growth conditions, and a short period of chilling. In fact, the very cause of the disorders is less the insufficient chilling avalaible than the double action of these low temperatures that partly increase at first the depth of dormancy before starting to eliminate it.
Table des matières
1. Introduction
1Au Maroc, les régions où les besoins en froid du pommier peuvent être satisfaits sont très limitées (Zguigal, Chahbar, 1993). Par ailleurs, plusieurs observations au champ permettent de considérer que le manque de froid se pose d’une façon très importante. En effet, le taux de débourrement atteint seulement 15 % et 30 % respectivement chez les cultivars Golden delicious et Reine des Reinettes cultivés dans la région du Gharb (Ben Ismail, 1981) et 52,9 % chez Golden delicious dans la région de Meknès (Taoura, 1986 ; Zguigal, 1992).
2Or, la culture du pommier est en pleine expansion au Maroc. Les variétés cultivées, introduites essentiellement de l’étranger, manifestent des symptômes d’inadaptation climatique : débourrement retardé, erratique et incomplet.
3Le comportement automno-hivernal de leurs bourgeons conditionne, d’une manière variable, l’aptitude des arbres à pousser et à fructifier, selon l’impact d’influences multiples et simultanées de facteurs intrinsèques et extrinsèques à la plante.
4La connaissance de l’évolution de l’inertie des bourgeons et des caractéristiques de leur débourrement est indispensable et constitue une base de la compréhension de certaines expressions morphologiques de l’arbre. On conçoit tout l’intérêt que présente, dans son ensemble, la connaissance des phénomènes physiologiques liés à la période de repos végétatif. En effet, il est nécessaire de connaître le déterminisme physiologique pour mieux comprendre l’action des facteurs climatiques sur l’évolution du repos afin de pouvoir le contrôler et de le modifier éventuellement.
5L’objectif de ce travail consiste à suivre l’évolution des capacités intrinsèques de débourrement du bourgeon durant la phase automno-hivernale.
2. Matériel et méthodes
2.1. Matériel
6Le matériel d’étude est constitué par des arbres adultes de pommier (Malus x domestica Borkh), cv : Golden delicious, conduits en gobelet, dans la région de Meknès.
2.2. Méthodes
7L’étude des caractéristiques de débourrement est conduite sur des bourgeons isolés en boutures de nœuds (Nigond, 1967 ; Crabbé, 1968). L’étude de la cinétique de dormance a porté sur les cycles suivants : 1990–1991, 1991–1992 et 1992–1993.
8Durant les périodes estivale et hivernale des deux premières années de l’étude, nous avons noté les particularités de croissance de chaque rameau : dates approximatives d’arrêt et de reprise éventuelle de la croissance, d’arrêt définitif de la croissance et de chute des feuilles. Pour la troisième année seule la date de chute des feuilles a été notée.
9Technique de boutures de noeuds isolés (BNI). Des rameaux à une vague de croissance sont prélevés à intervalles plus ou moins réguliers (deux à trois semaines) de la mi-juillet à avril. Les boutures de 5 à 6 cm portant chacune un bourgeon en position distale, sont obtenues à partir de ces rameaux. Les autres bourgeons situés sur la bouture sont supprimés au scalpel.
10Après paraffinage de leur extrémité supérieure et des cicatrices des bourgeons enlevés, les boutures sont plantées dans des caisses remplies d’une couche de tourbe recouverte d’un mélange de perlite et de sable préalablement stérilisé. Ce milieu de culture est maintenu constamment humide par des apports d’eau réguliers. Les caisses sont, par la suite, placées en enceinte climatisée (température constante de 20 °C ± 2, jours longs de 16 heures).
11Les observations sur le débourrement se font quotidiennement pour les bourgeons isolés, et ce pendant une durée de 60 jours. Nous avons considéré comme débourré tout bourgeon gonflé laissant apparaître la couleur verte des jeunes feuilles à travers les écailles.
12Expression des résultats. L’état d’inertie d’une population des bourgeons à un instant donné est caractérisé par deux paramètres :
13- le « temps moyen de débourrement » (TMD) exprimé en jours (Nigond, 1967). Ce paramètre n’est autre que l’inverse de la vitesse moyenne de développement, c’est-à-dire la moyenne harmonique des délais individuels de débourrement des bourgeons observés au cours de leur culture à 20 °C. Schématiquement, plus le TMD est élevé, plus la dormance est profonde.
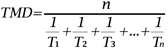
14où n est le nombre total de bourgeons du lot ; T1, T2, ... Tn sont respectivement les temps, en jours, nécessaires au débourrement du 1er, 2ème, ... nème bourgeon. Les bourgeons n’ayant pas atteint le stade de débourrement, après 60 jours de culture, sont notés comme ayant un délai de débourrement infini.
15- Le nombre maximal de bourgeons débourrés (DM) donné en pourcentage de débourrement par rapport au nombre total d’individus testés. Il permet d’apprécier la capacité de débourrement d’un lot de bourgeons.
162.3. Données climatiques
17L’accumulation des heures de froid inférieures à 7, 2 °C, calculées selon la formule :
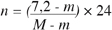
18où n = nombre d’heures de froid ; M et m = températures moyennes maximales et minimales journalières (Weinberger, 1950), dans la nature a commencé à partir du 23 octobre pour le premier cycle, du 30 octobre pour le deuxième cycle et du 11 novembre pour le troisième cycle. Nous avons enregistré, de septembre à fin avril, 750, 1 ; 701, 7 et 761, 6 heures de froid respectivement en 1990–1991, 1991–1992 et 1992–1993.
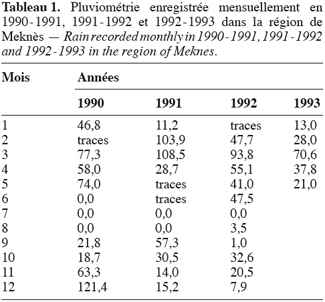
19La pluviométrie enregistrée du mois d’avril jusqu’au mois de mars est de 580, 8 mm en 1990–1991, de 287, 5 mm en 1991–1992 et de 320, 7 mm en 1992–1993 (Tableau 1).
20La photopériode passe, à la latitude de Meknès, de 12 heures à 9 heures 30 min, de septembre à décembre, et de 9 heures 30 min à 13 heures de décembre à mai.
3. Résultats
3.1. Croissance des rameaux
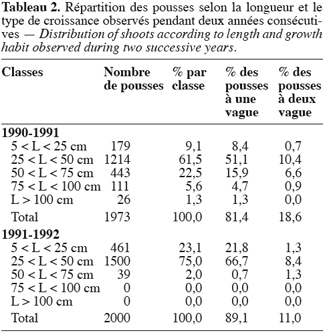
21La distribution des pousses par classe de longueur et par type de croissance (Tableau 2) montre que : les rameaux à une vague de croissance représentent plus de 80 % des pousses observées ; la longueur moyenne diffère d’une année à l’autre ; et le pourcentage des pousses ayant une deuxième vague d’allongement varie selon les années. En effet, en 1991–1992 la majorité des rameaux (98 % contre 70, 6 % en 1990–1991) avaient une longueur inférieure à 50 cm et le taux de ceux qui ont présenté deux vagues d’allongement était de 11 % seulement (contre 18, 6 % en 1990–1991).
22La croissance des pousses à une vague d’allongement s’arrête généralement vers la fin du mois de juin. Celle des pousses à deux vagues de croissance reprend entre la deuxième décade de juillet et le mois d’août, et s’achève vers fin août - début septembre.
3.2. Chute des feuilles
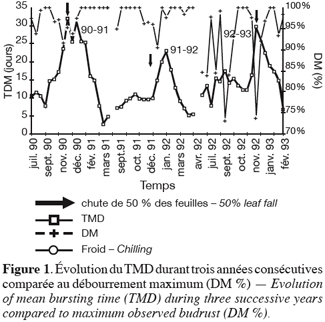
23La chute des feuilles commence généralement vers la mi-novembre. La date où 50 % des feuilles ont chuté est indiquée par une flèche sur les figures 1 et 2. Elle correspond au 20 décembre en 1990–1991, au 13 décembre en 1991–1992 et au 24 décembre en 1992–1993. Les feuilles au-delà restantes, ne sont probablement plus actives.
24Par rapport au comportement en régions tempérées plus septentrionales, on peut souligner : la tardiveté de cette chute ; l’étalement de la période de chute : près de deux mois (de mi-novembre à janvier) contre une à deux semaines au début novembre en Belgique ; la similitude des conditions extérieures au moment où 50 % des feuilles sont tombées : photopériode d’environ 10 heures et premières unités de températures inférieures à 7, 2 ° C.
3.3. Variation dans le temps de la cinétique de dormance des bourgeons
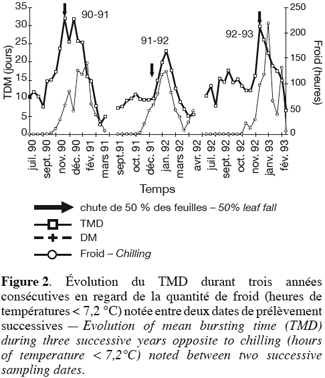
25Les trois années d’expérimentations fournissent une image assez complète de la manière dont se déroule la dormance des bourgeons, en climat à hiver doux (Figures 1 et 2).
26Un premier fait à souligner est que le niveau de dormance (TMD) atteint, dans ces conditions, est faible, si on le compare à la situation observée dans les régions plus septentrionales (France, Belgique). Dans ces dernières, on atteint des profondeurs de dormance telles que plus aucun débourrement n’est obtenu sur boutures de bourgeons isolés à des températures voisines de 20–25 °C, alors que, dans nos conditions, les TMD maximums excèdent à peine 30 jours et les taux de débourrement restent fort élevés (75 % minimum lors de la dormance 1992–1993, la plus profonde, et plus de 90 % les autres années).
27Une autre remarque concerne les courbes de débourrement présentées dans la figure 3. Ces courbes sont en général très redressées, le passage de 20 à 80 % de débourrement se réalise, à de rares exceptions près, court et voisin de 5 jours. Le comportement des bourgeons d’un même prélèvement est donc homogène. Les exceptions appartiennent à des échantillons de bourgeons prélevés au plus profond de la dormance, où l’hétérogénéité de comportement se marque aussi par un débourrement incomplet de l’échantillon. Toutefois, l’homogénéité de comportement observée, pendant la plus grande part de l’évolution automno-hivernale des bourgeons, nous permet de considérer comme significatives des différences de TMD, dès qu’elles dépassent 5 jours environ.
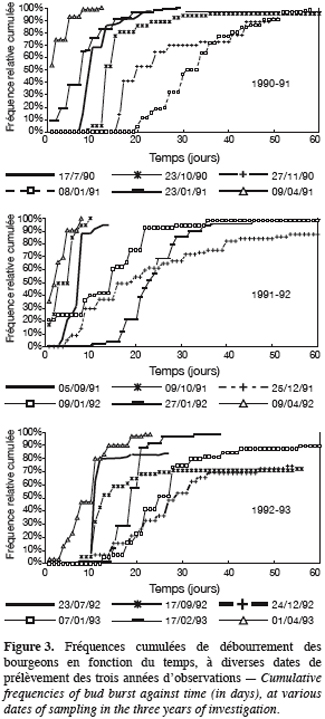
28La comparaison des trois années d’expérimentation fait ressortir l’importance de trois faits, dans le déroulement de la dormance : l’état initial de dormance des bourgeons entre août et octobre, les conditions de la montée en inertie et celles de l’effacement de la dormance. Ces trois faits sont en relation étroite.
29En effet, on peut dire que, grosso modo : 1990–19 91 et 1991–1992 sont caractérisées par un état initial à faible TMD (10 jours), 1992–1993 partant avec une inertie déjà plus élevée (15 jours) ; 1990–1991 et 1992–1993 atteignent une dormance maximale plus profonde (TMD de 30 jours) que 1991–1992 (TMD de 23 jours). On peut noter ces différences sur les courbes d’évolution du TMD au cours du temps (Figure 2), ainsi que leurs transposition sur les courbes de fréquence de débourrement (Figure 3).
30Cependant, en regardant de plus près les courbes d’évolution du TMD, d’autres similitudes et différences se remarquent. En 1990–1991 et 1991–1992, les circonstances de la montée en inertie sont différentes. Partant d’un niveau également bas de TMD, l’augmentation de la dormance en 1990–1991 commence en début novembre, alors qu’il n’y a pas encore eu de froid (t ° < 7, 2 ° C), et va devenir plus profonde encore, avec le concours des premiers froids. Par contre, en 1991–1992, la dormance s’intensifie un mois plus tard et suit l’accumulation d’heures de froid. Le tableau 1 nous permet, par ailleurs, de constater qu’en 1990–1991 la croissance des 29 % des rameaux dépassent 50 cm de longueur contre 2 % mais aussi 18 % contre 11 % manifestent une seconde vague de croissance.
31En 1992–1993, comme en 1991–1992, ce sont les premiers froids qui vont accentuer la dormance, mais, l’état initial d’inertie étant plus élevé, elle devient plus profonde, autant qu’en 1990–1991 bien que s’installant plus tardivement. Les courbes de débourrement révèlent d’ailleurs, pour cette année-là, les plus grandes hétérogénéités de comportement des bourgeons, avec les temps de latence les plus longs et les taux de débourrement réduits (Figure 3).
32Notons encore que la quantité de froid accumulée, avant que le TMD maximal ne soit atteint, est de 98, 5 ; 445, 2 et 158,1 heures respectivement en 1990–1991, 1991–1992 et 1992–1993. Dans la phase de la diminution de la dormance, il y a eu 634, 7 heures en 1990–1991, 238, 4 heures en 1991–1992 et 577, 7 heures en 1992–1993.
4. Discussion et conclusion
33L’évolution des temps moyens de débourrement, observés de juillet à avril, montre une remarquable similitude, au cours des trois années d’investigations. Les courbes obtenues présentent deux pics d’inertie des bourgeons.
34Le premier de ces pics, relativement faible, culmine vers octobre, à un moment où, sous le climat de Meknès, des températures basses sont rarement notées. L’inertie des bourgeons s’y montre toutefois variable d’une année à l’autre : il est vraisemblable que l’intensité du phénomène est influencée par des conditions de croissance antérieure. Ce pic peut d’ailleurs être modifié par des atteintes à cette croissance, telles que taille ou défoliation (Zguigal, 1995).
35Cependant, des différences notables apparaissent au niveau de la date de début de l’intensification de la dormance et de la valeur maximale du TMD. En effet, les résultats obtenus indiquent que selon les années, les variations de la courbe de dormance sont fonction non seulement du moment où se déroulent les changements dans l’intensité de la dormance mais également de la vitesse avec laquelle ces changements se produisent. Nous nous trouvons là dans la phase qui va de la formation des bourgeons à leur inaptitude croissante à débourrer, consécutives aux variations de l’allocation des ressources, surtout glucidiques, liées à la compétition créée par l’activité cambiale prolongée et par la constitution de réserves dans les rayons parenchymateux (Parmentier et al., 1991 ; Ricaud et al., 1991 ; Barnola, Crabbé, 1993). Cette inertie d’origine corrélative (premier pic) peut se maintenir ou disparaître partiellement, mais constitue comme un stade préalable à la dormance vraie (Arias, Crabbé, 1975 ; Crabbé, 1984 ; Latimer, Robitaille, 1981 ; Mauget, 1982).
36C’est lorsque commencent de s’accumuler les heures de froid (novembre), que l’inertie des bourgeons se renforce fortement et que la courbe des TMD va vers un second pic nettement plus marqué, culminant vers janvier. Les températures basses étant alors presque continues, la dormance s’élimine ensuite progressivement. Le double rôle du froid, susceptible d’accentuer, puis de lever une dormance (Lavarenne et al., 1975), est dans nos résultats remarquablement mis en lumière.
37Le cycle 1992–1993 est à cet égard particulièrement éclairant. La conjonction d’un stade initial (premier pic) d’inertie élevée et d’une arrivée plus tardive du froid y entraîne l’installation d’une dormance, certes pas plus profonde, mais à élimination lente : ce n’est que grâce à un coup de froid de mars que le TMD revient à une valeur de cinq jours.
38Les disparités de quantité de froid accentuant et effaçant l’inertie des bourgeons au cours des trois années d’observations suggèrent que ces deux phases, d’accentuation et d’effacement de l’inertie des bourgeons, sont relativement indépendantes et différemment conditionnées par des événements internes et externes. Le contexte différent de croissance, avec les conséquences qu’il entraîne au plan du métabolisme et de l’allocation des ressources, peut expliquer la précoce montée en inertie des bourgeons en 1990–19 91.
39Ainsi, il apparaît que la cause du débourrement erratique et incomplet, observée en climat à hiver doux, résulte moins d’un froid insuffisant que de l’inefficacité des premiers froids, qui accentuent la dormance et ne l’éliminent pas encore.
40Terminons par la comparaison de diverses situations (Figure 4) : selon Arias, Crabbé, 1975 ; Mauget, 1976, 1982, 1987 ; Mauget, Rageau, 1988, en régions tempérées, la montée de l’inertie de fin août-septembre, est tout de suite accentuée par les unités de froid (et sans doute aussi par le raccourcissement très rapide de la photopériode). Les deux pics sont présents, mais tendent à se confondre. Mais, les froids s’accentuant en novembre-décembre, et la sensibilité du bourgeon se modifiant, cette dormance est alors progressivement effacée. Elle a pratiquement disparu déjà en janvier et est remplacée par une quiescence des bourgeons (qui ne demandent plus que chaleur, absente à ce moment, pour débourrer).
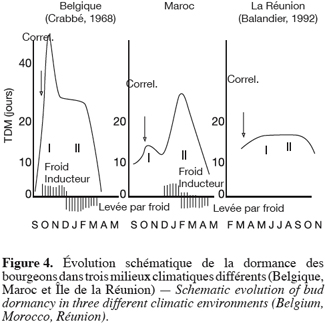
41En climat tropical, sur l’île de la Réunion (Balandier, 1992 ; Balandier et al., 1992), une période d’inertie faible, avec des TMD inférieurs à 15 jours, se développe, mais qui n’est jamais accentuée par des températures basses inexistantes même en altitude. Cette inertie a d’abord une origine corrélative (premier pic). Elle acquiert néanmoins finalement les caractères d’une dormance vraie (sensibilité au froid, incapacité à faire des nucléotides).
42En général, donc, les étapes de la dormance se succèdent de la façon suivante :
43a) Phase I : établissement de la dormance succédant à l’inhibition par corrélations (dominance apicale, feuilles, axe, etc.) ;
44b) Renforcement et stabilisation de cette dormance par les jours courts et les premiers froids ;
45c) Phase II : dormance proprement dite levée par le froid ;
46d) Situation de quiescence en attente des températures tièdes.
47Au Maroc, pays à climat méditerranéen : l’étape (b) intervient tard par rapport à la situation belge. A la Réunion, elle ne survient peut-être jamais. La brève phase de dormance vraie observée, dans cette île, par Balandier (1992) pourrait être due à la longue privation de l’irrigation qui la précède. Le stress hydrique jouant alors un rôle identique à celui du froid inducteur ; l’étape (d) n’est pas perceptible, la disparition de la dormance débouchant tout de suite sur des températures compatibles avec le débourrement.
48Deux situations opposées s’observent donc : dormance profonde mais relativement labile, en régions à hiver rude, et dormance faible mais plus stable (Zguigal, 1992, 1995) en régions à hiver doux. Elles s’expliquent par la succession d’une inertie d’origine corrélative, installée dans les circonstances de l’arrêt de la croissance, et d’une dormance vraie, sous la dépendance du double rôle joué par les températures basses.
49Par rapport aux climats à hiver plus rude, nous n’avons pas observé de différence marquante quant au déroulement même de la croissance : à une vague de croissance printanière s’achevant vers fin juin - début juillet, succède une vague de croissance estivale qui se termine en septembre. Toutefois, malgré l’irrigation, cette croissance est moins vigoureuse ; les rameaux restent plus courts et les deuxièmes vagues sont plus rares.
50Par contre, le feuillage reste apparemment beaucoup plus longuement actif, sa sénescence est retardée et l’abscission s’étale de mi-novembre à fin décembre. Par comparaison, en Belgique, la chute des feuilles s’accomplit en une à deux semaines, en début novembre.
51Ce feuillage longuement persistant peut avoir des effets variés, tel la fourniture prolongée de glucides par photosynthèse, la concurrence accrue et prolongée pour l’eau, vis-à-vis des bourgeons et des rameaux ou la production éventuelle d’ABA.
52Cependant, beaucoup reste à faire pour comprendre le mécanisme de ces phénomènes. Il est clair, en effet, que l’accentuation comme l’élimination de la dormance sont malaisées à mettre en rapport avec la quantité de froid reçu, pour les raisons classiquement invoquées de méconnaissance d’une date initiale de ces actions. Les travaux classiques ignorent et négligent d’ailleurs le plus souvent l’effet d’accentuation. Quant aux chercheurs qui ont mis en évidence ce dernier effet, ils sont de plus en plus amenés à penser que l’action du froid et des températures en général, sur les bourgeons est multiple avec des organes récepteurs ou des processus sensibles différents et en interaction (Crabbé, 1994 ; Crabbé, Barnola, 1996).
Bibliographie
Arias O., Crabbé J. (1975). Les gradients morphogénétiques du rameau d’un an des végétaux ligneux, en repos apparent. Données complémentaires fournies par l’étude de Prunus avium L. Physiol. Vég. 13 (1), p. 69–81.
Balandier P. (1992). Etude dynamique de la croissance et du développement des bourgeons de quelques cultivars de pêcher, cultivés à diverses altitudes sous le climat tropical de l’île de la Réunion. Thèse Dr. Univ. Clermont-Ferrand, 90 p.
Balandier P., Capitan F., Quignot S., Rageau R., Parisot E. (1992). Etude de la croissance et du développement des bourgeons du pêcher cultivé à l’île de la Réunion : application à l’élaboration d’un itinéraire cultural. Fruits 47 (6), p. 679–689.
Barnola P., Crabbé J. (1993). L’activité cambiale, composante active ou passive dans les réactions de croissance de l’arbre ? Acta Bot. Gallica 140 (4), p. 403–412.
Ben Ismail MC. (1981). Contribution à l’étude de la dormance des bourgeons et de l’effet de leur forçage chez le pommier (cv Reine des Reinettes et Golden delicious) dans le Gharb. Mémoire de 3e cycle. Agronomie, IAV. Hassan II Rabat, Maroc.
Crabbé J. (1968). Evolution annuelle de la capacité intrinsèque de débourrement des bourgeons successifs de la pousse de l’année chez le pommier et le poirier. Bull. Soc. Roy. Bot. Belg. 101, p. 195–204.
Crabbé J. (1984). Correlation effets modifying the course of bud dormancy in woody plants. Zeitsch. Pflanzenphysiol. 113 (5), p. 465–469.
Crabbé J. (1994). Dormancy. In Encyclopedia of Agriculural Science (vol.1). New York: Academie Press, p. 597–611.
Crabbé J., Barnola P. (1996). A new conceptual approach to bud dormancy in woody plants. In G. Lang (ed.). Plant dormancy. Wallingford (UK): CAB International, p. 83–113.
Latimer J., Robitaille HA. (1981). Sources of variability in apple shoot selection and handling for bud rest determinations. J. Amer. Soc. Hort. Sci. 106 (6), p. 794–798.
Lavarenne S., Champagnat P., Barnola P. (1975). Influence d’une même gamme de températures sur l’entrée et la sortie de dormance des bourgeons du frêne (Fraxinus excelsior L.). Physiol. Vég. 13 (2), p. 215–224.
Mauget JC. (1976). Sur la dormance des bourgeons végétatifs du noyer (Juglans regia L.). C. R. Acad. Sci., Paris 283, p. 499–502.
Mauget JC. (1982). Relation entre dormance et précocité de débourrement des bourgeons du noyer (Juglans regia L.) : Influence du génotype et du milieu. 2e Colloque sur les Recherches Fruitières. Bordeaux, p. 95–106.
Mauget JC. (1987). Dormance des bourgeons chez les arbres fruitiers de climat tempéré. In Le Guyader H. (éd.). Le développement des végétaux. Paris : Masson, p. 133–150.
Mauget JC., Rageau R. (1988). Bud dormancy and adaptation of apple tree to mild winter climates. Acta Hortic. 232, p. 101–108.
Nigond J. (1967). Recherches sur la dormance des bourgeons de la vigne. Ann. Physiol. Vég. 9 (1), p. 102–107 ; 9 (2), p. 197–232 ; 9 (3), p. 273–338 ; 9 (4), p 397–414.
Parmentier C., Barnola P., Maillard P., Lavarenne S. (1991). étude de croissance rythmique du chêne pédonculé. Influence du système racinaire. In Edelin C. (éd.). L’Arbre. Biologie et développement. Actes du 2e Colloque international sur l’Arbre, Montpellier 10-15 septembre 1990. Naturalia Monspeliensia, HS. A7, p. 327–343.
Ricaud S., Barnola B., Botton B. (1991). Physiologie de l’arbre d’alignement en ville : dormance et croissance des bourgeons de Platane. In: Edelin C. (éd.). L’Arbre. Biologie et développement. Actes du 2e Colloque international sur l’Arbre, Montpellier 10-15 septembre 1990. Naturalia Monspeliensia, HS. A7, p. 650–651.
Taoura M. (1986). Etude des effets de la levée artificielle de la dormance chez le pommier « Golden delicious » dans la région de Saïs : Utilisation du DNOC et de l’huile de pétrole. Mémoire de 3e cycle Agronomie , IAV. Hassan II Rabat, Maroc, 106 p.
Weinberger JH. (1950). Chilling requirements of peach varieties. Proc. Amer. Soc. Hort. Sci. 56, p. 122–128.
Zguigal Y. (1992). Etude de la dormance des bourgeons du pommier et influence des produits chimiques de levée de dormance. Mémoire d’ingénieur en chef, Rabat : INRA, 64 p.
Zguigal Y. (1995). Evolution et caractéristiques de la dormance des bourgeons du pommier (Malus x domestica Borkh., cv Golden delicious) dans un climat à hiver doux (région de Meknès, Maroc). Thèse doct. Sci. agron., IAV. Hassan II. Rabat, Maroc, 164 p.
Zguigal Y., Chahbar A. (1993). Carte des heures de froid au Maroc. Al Awamia 80, p. 161–171.
Pour citer cet article
A propos de : Amina Zguigal
Agronomie et Physiologie végétale, INRA, BP 415 Rabat (Maroc). E-mail : zguigal@yahoo.fr
A propos de : Abdelhak Chahbar
Département de l’Amélioration et de la Conservation des ressources génétiques, INRA, BP 415 Rabat (Maroc).
A propos de : Dou-El Makan Wallali Loudiyi
Institut agronomique et vétérinaire Hassan II, Département d’Horticulture, BP 6202 - Instituts, 10101 Rabat (Maroc).
A propos de : Jacques Crabbé
Faculté universitaire des Sciences agronomiques de Gembloux, Passage des Déportés, 2, B-5030 Gembloux (Belgique).





